- 前列腺癌(Prostate cancer, PCa)肿瘤生物学基础的学习笔记
- 课程链接:https://www.bilibili.com/video/BV1Dj411R73C
1. 生物基础
1.1 前列腺癌
- 前列腺 (Prostate)
- 一种男性的腺体器官,核桃大小,位于膀胱下方;
- (1) 防止尿路感染;(2) 产生的Prostate Specific Antigen (PSA, 前列腺特异性抗原) 蛋白酶可以帮助液化精液 (与勃起、生殖无关)。
- 良性前列腺增生 (Benign Prostatic Hyperplasia, BPH)
- 随着年龄增长而表现出的前列腺增大,导致排尿困难;
- 它不是前列腺癌的诱发因素。
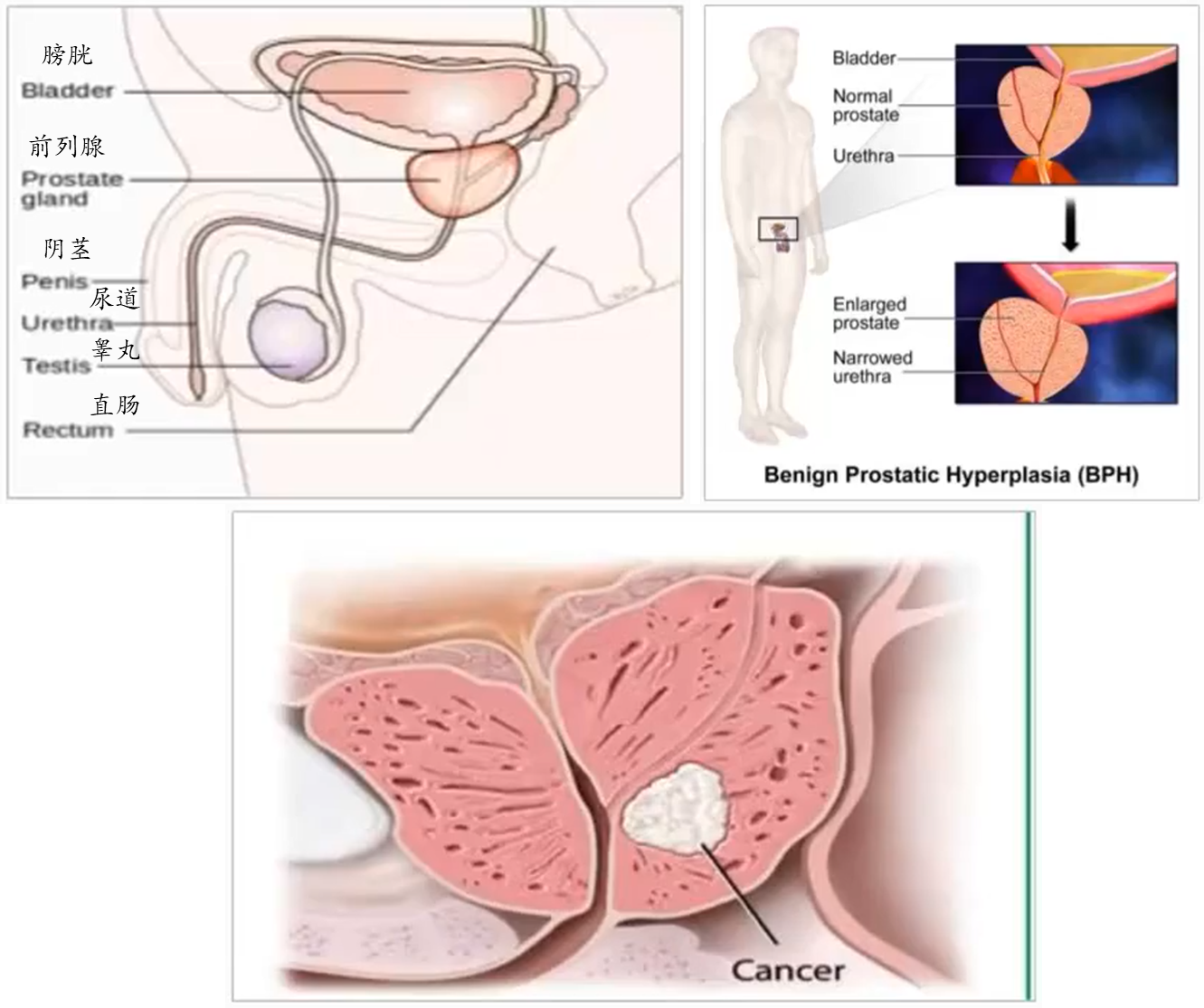
- 前列腺癌(Prostate Cancer, PCa)
(1)发病率
- 男性最常见的癌症之一,每年有22万人确诊(美国)
- 每年全球有110万男性确诊为PC,约占男性癌症的15%
- 男性致死率第二的肿瘤类型,每年有2.7万人死于PC(美国)
- 每年全球约有30万死于PC,约占男性死亡的6.6%(第五)
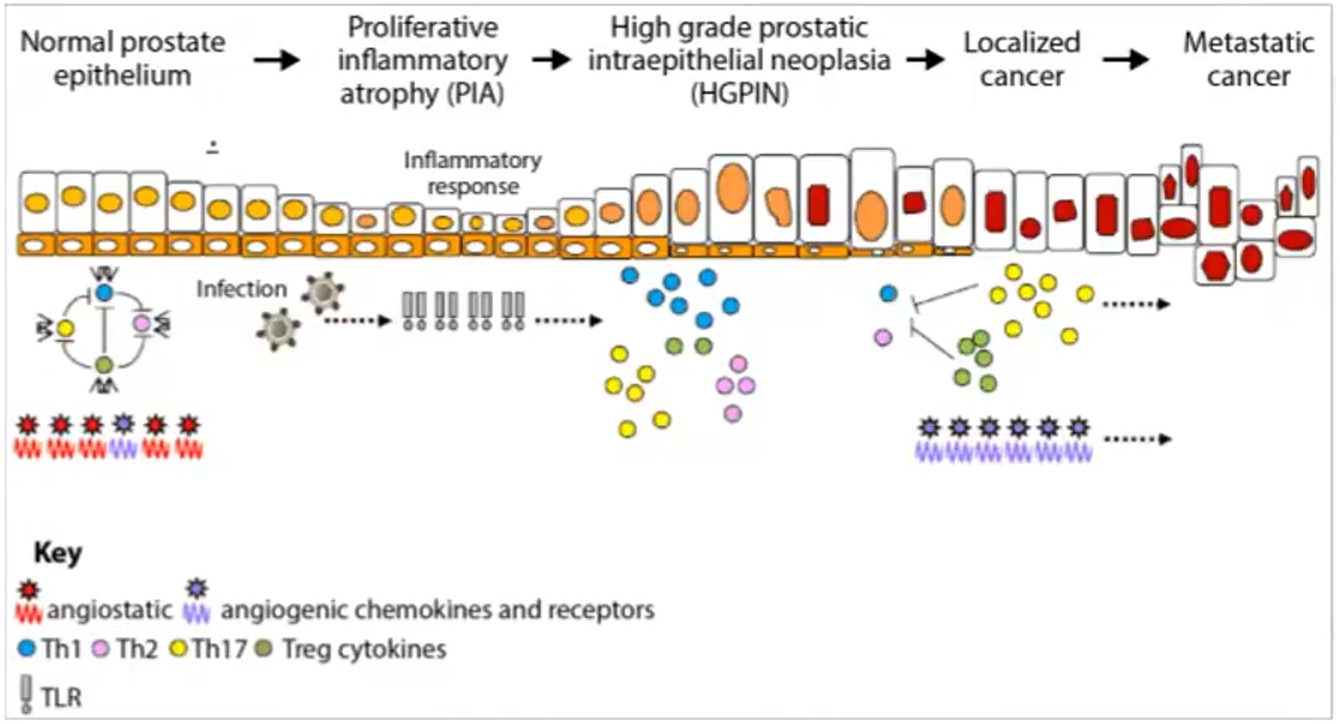
(2)发展历程
1)正常前列腺上皮细胞;主要由基底细胞和分泌细胞组成;
2)增生性炎性萎缩(PIA):细胞萎缩(体积减小)但伴随不正常的增殖。炎症细胞的浸润(如淋巴细胞)在局部可见;
3)高级别前列腺上皮内瘤变(HGPIN):异常增生的上皮细胞(核增大等),但尚未侵入基底膜,因此还没有形成真正的癌症;
4)局限性PCa:细胞突破基底膜,但仍局限于前列腺内部,尚未扩散到周围组织或远处器官;
5)转移性PCa:癌细胞扩散到前列腺外的其他组织或器官。
(3)风险因素
- 年龄:多发于老年男性。60%诊断于65岁以上男性,较少在40岁以下男性中发现;
- 种族:多发于非遗美国人,少见于亚洲男性
- 家族史:有较显著遗传倾向,父亲或兄弟确诊的男性发病率翻倍
- 基因:HOXB13,BRCA1/2,MSH2,MLH1
- 饮食:多吃红肉、少吃蔬菜的发病率更高
1.2 癌症特征
(1)What is cancer:
- “Uncontrolled growth”: 体内某些异常细胞的不受控制的分裂;
- 也称为Tumor,由组织异常生长(良性/恶性)引起的身体某个部位的肿胀,通常没有炎症;
- 也称为Neoplasm,描述了体内组织的任何新的和异常的生长。
(2)How cancer can be classifed by the originated tissue
- Carcinoma,起源于上皮组织,有两种常见亚型
- Adenocarcinomas腺癌:源自腺体的上皮细胞,腺体是分泌物的组织(如乳腺、前列腺、胃腺等);
- Squamous cell carcinomas鳞状细胞癌:源自鳞状上皮细胞,这种细胞常见于皮肤和许多内脏器官的表面。
- Sarcoma肉瘤:起源于间叶组织,包括结缔组织、肌肉、脂肪、血管和淋巴组织等
- Leukemia白血病:起源于骨髓中
- Lymphoma淋巴瘤:起源于淋巴系统
(3) Genetic Disease
- 癌症由基因组的异常突变累积导致,单基因突变通常不会引起;
- 例如:
- 一个抑癌基因(tumor suppressor gene)发生突变,导致失活。
- 负责DNA修复的基因发生突变,导致更多突变;
- 致癌基因(Oncogene)发生突变,细胞快速增殖
(4)Cancer Hallmarks
- 肿瘤细胞可以刺激它们的生长;
- 抵抗抑制信号;
- 抵抗程序性细胞死亡;
- 无限繁殖;
- 刺激血管生成;
- 侵入邻近组织,转移到远端组织;
- 异常的代谢通路(能量 )
- 逃避免疫系统
- 基因组不稳定
- 与炎症相关
2. 筛查与诊断
2.1 筛查手段
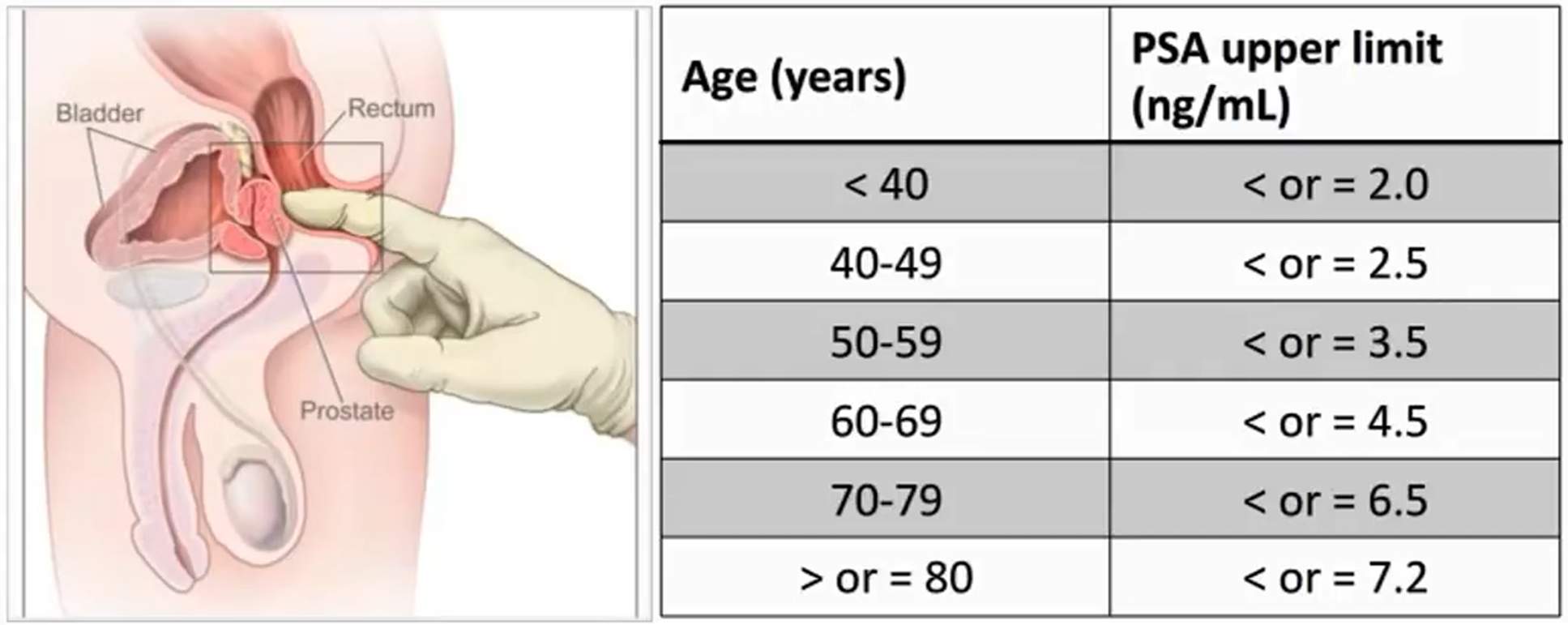
(1)DRE(肛肠指检)
- 50岁以上,每年DRE
- 使用手指感受前列腺处是否有肿
(2)PSA检查
-
检测血液中PSA含量,单位通常为(ng/mL)
-
55-69岁之间,正常范围是4ng/mL,年轻(<50)男性样本应低于2.5
-
争议:高水平的PSA含量不一定是PC,只有25%高PSA男性被确诊为前列腺癌(过度筛查)
-
改进版的PSA评估
- Free versus total PSA (‘Free’: not bound to other proteins)
- 较低的比值(小于0.1),即更少的Free PSA与Aggressive cancer更相关;
- Age-specific的PSA含量阈值:年老的患者的阈值更高
- PSA velocity:每年PSA含量的变化(>0.7 )
- PSA doubling:PSA含量提高一倍时的时间窗口
- Free versus total PSA (‘Free’: not bound to other proteins)
(3)PHI, Prostate Health Index →相比前者better predictor
- 基于free PSA,total PSA,[-2]proPSA isoform of free PSA三者的组合。
- ProPSA,特别是[-2]proPSA,具体指的是一种PSA的前体形式。
(4)4Kscore
- 基于4种kallikrein(激肽释放酶)的检测结果及临床信息进行打分
- 与PSA相关的指标相互补充,更适合用于aggressive PC
2.2 诊断方式
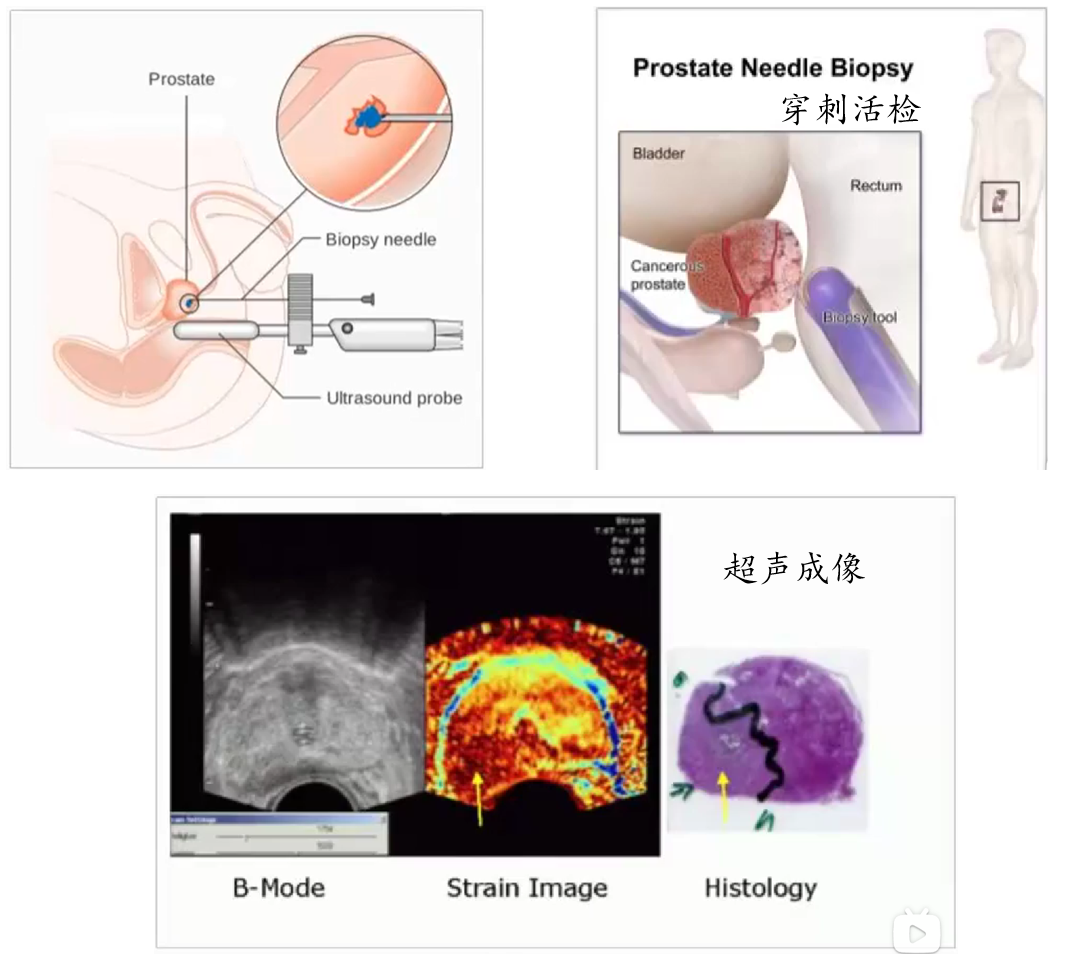
- 超声成像检查(Ultrasound)
- 将超声探头放置直肠内,对前列腺成像
- 穿刺活检(Needle Biopsies)
- 对前列腺不同区域,进行12处穿刺(对于穿刺异常的区域,会两次取样)
- 医生一般将前列腺分为 (1)外周区,(2)中间区,(3) 过渡区。PC一般发生于外周区,靠近直肠。
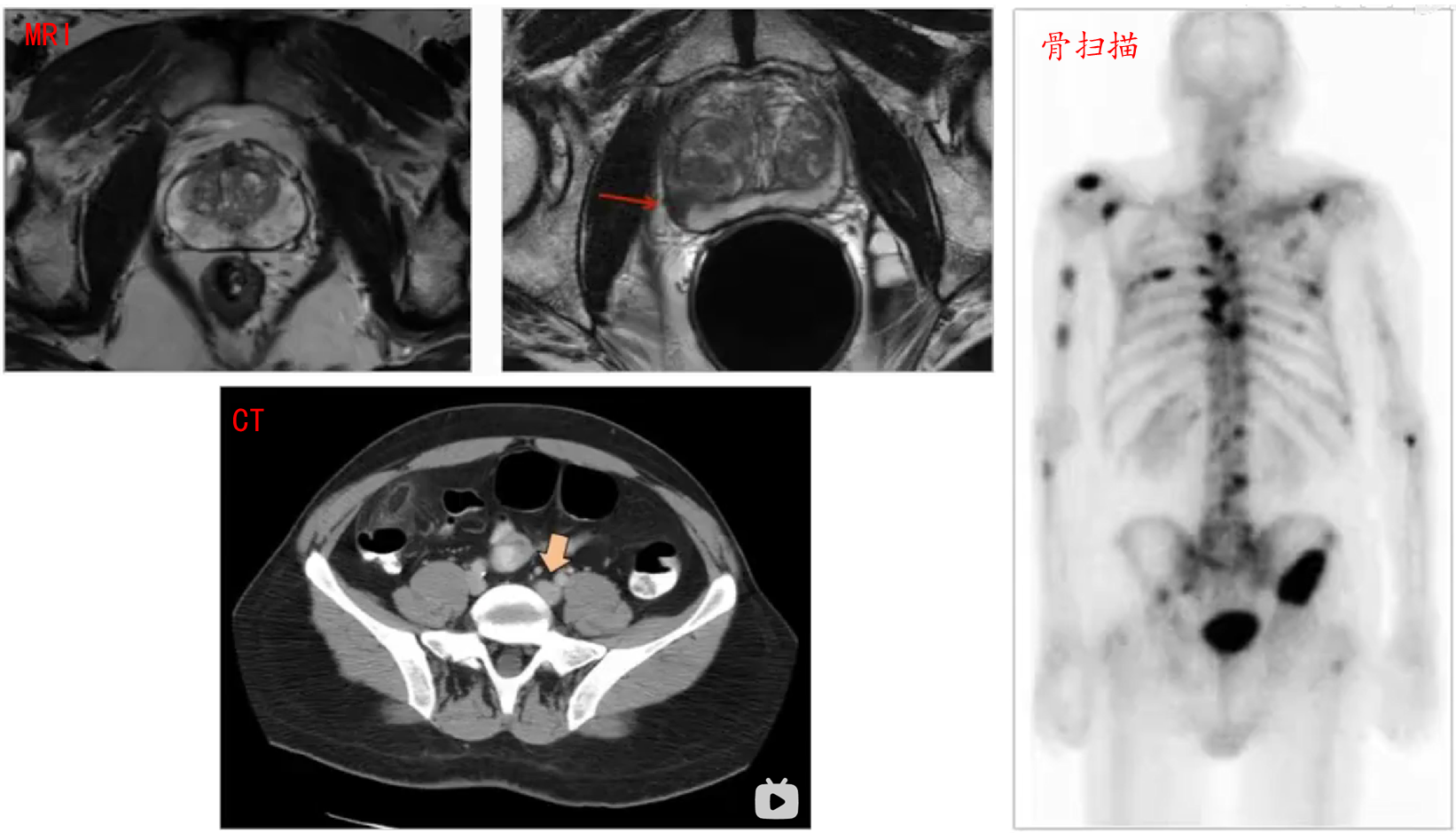
- 核磁共振(MRI):检查PC是否突破前列腺包膜,侵入其它周围组织
- CT扫描:观察淋巴结是否变大(可能是由于PC转移,也有可能是炎症等导致)
- 骨扫描/X-rays:观察是否存在骨损伤(可能是由于PC转移)
2.3 分期分级
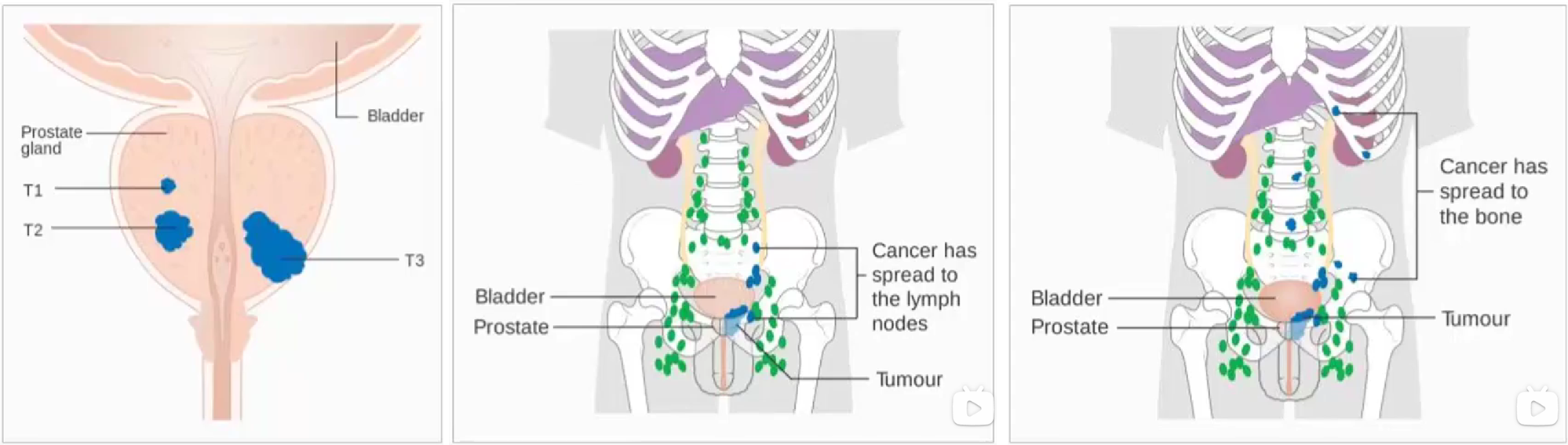
(1)TNM分期
- T = Tumor size
- T1c :通过PSA筛查发现
- T2 :局限性PC
- T3:突破前列腺包膜
- T4:进入到直肠或膀胱
- N = Lymph node involvement
- Nx:未进行相关检查
- N0:没有侵入淋巴结
- N1:存在侵入淋巴结
- N2、N3表示程度更高
- M = Presence of metastases
- Mx:未进行相关检查
- M1:发生了远端转移
- M1a:转移至骨盆(Pelvis)以外的淋巴结
- M1b:转移至骨
- M1c:转移到其它区域
(2)组织形态
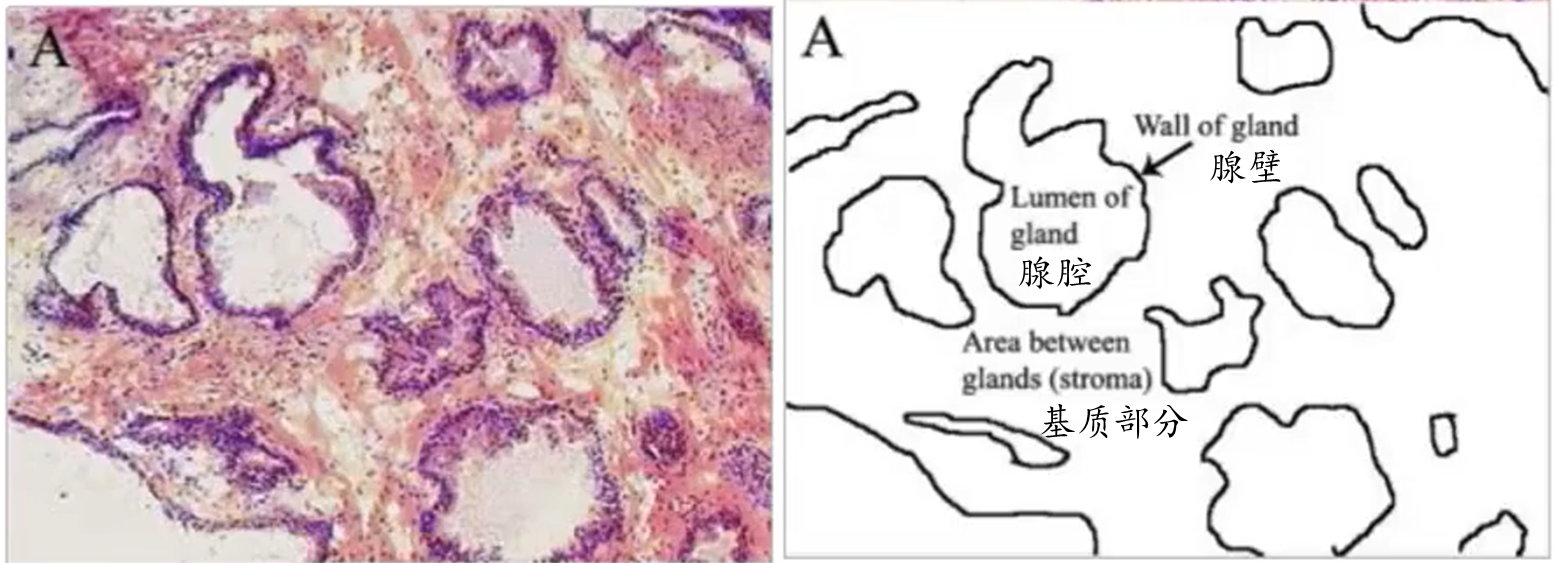
- 正常前列腺
- 腺体部分(glandular epithelium):包括前列腺腺泡(glandular acini)和导管,负责分泌前列腺液。
- 间质部分(stroma):主要由基质细胞(如成纤维细胞)、平滑肌细胞、血管、神经以及结缔组织组成。
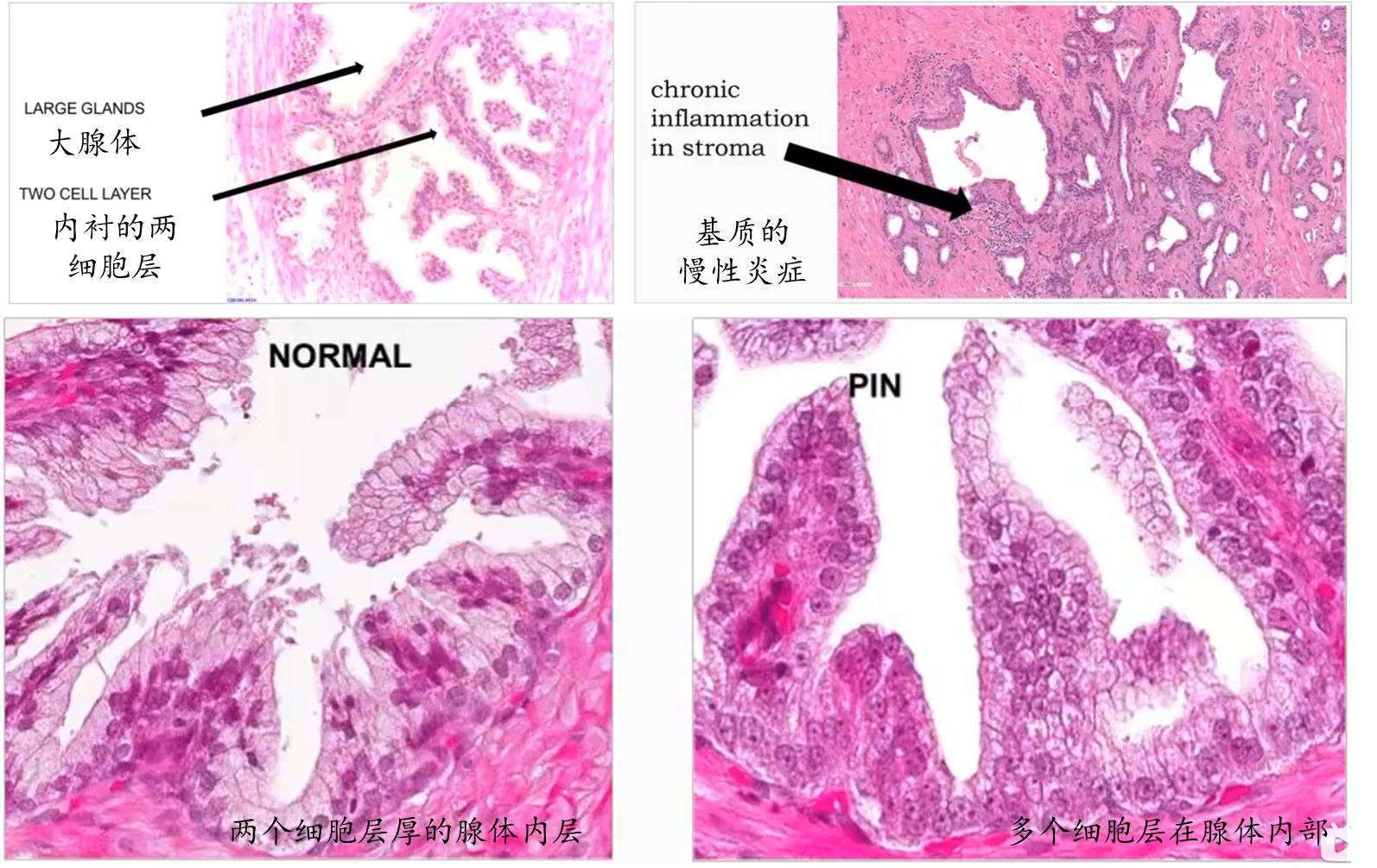
-
前列腺间质存在细胞炎症时
- 表现为细胞浸润(炎症细胞,包括淋巴细胞、巨噬细胞或浆细胞等)、纤维化和长期的组织反应
-
前列腺上皮内瘤变(PIN)
- 前列腺内的细胞异常增生情况。
(3)Gleason分数
-
Gleason分数用于评估前列腺癌分化程度,主要基于前列腺癌细胞的形态学特征,将腺体分化程度划分为五个等级:
-
1级:癌细胞分化较好,腺体结构基本保持正常;
-
2级:癌细胞分化较好,腺体结构出现一些不规则性;
-
3级:癌细胞分化较差,腺体结构明显异常,腺体边界不规则;
-
4级:癌细胞分化较差,几乎没有形成正常腺体的特征,明显的浸润性生长。
-
5级:癌细胞完全分化不良,几乎没有腺体结构,癌细胞成片生长,极具侵袭性。
-
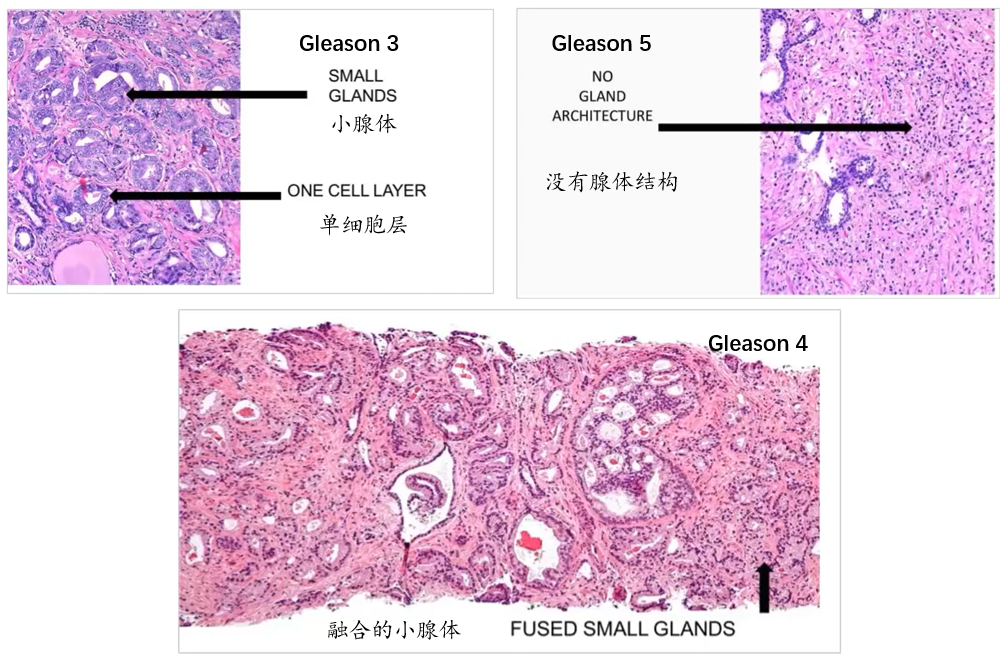
细胞分化是指细胞在生长过程中逐渐获得特定功能和形态的过程。
- 高度分化的细胞与其来源的正常组织细胞非常相似,形态较规则,仍保留了部分或大部分的正常功能。
- 生长速度慢;局限于原位,侵袭性弱;转移风险低等
- 低度分化的细胞则与正常细胞相去甚远,功能异常,形态不规则,表现出更强的恶性特征。
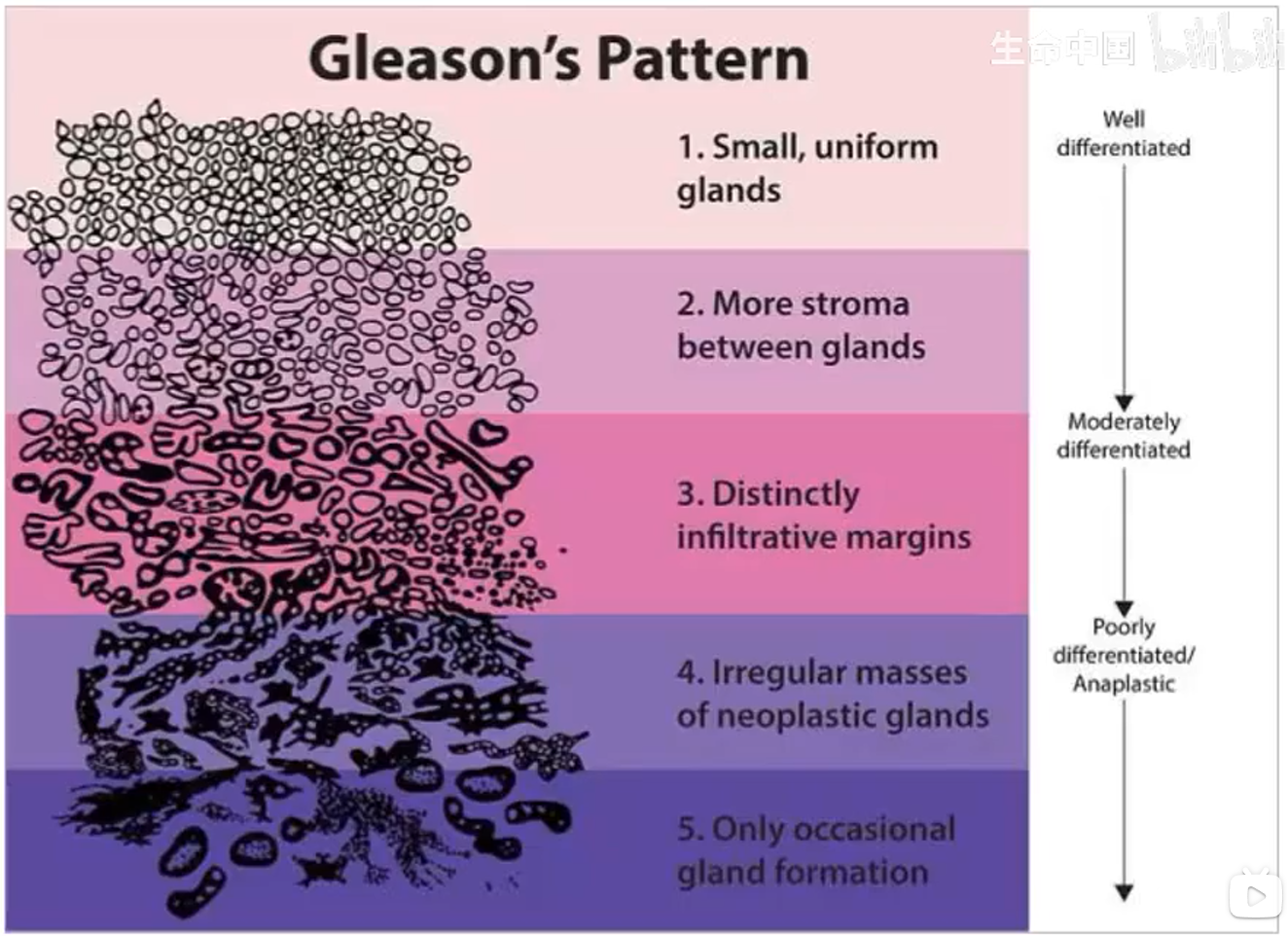
-
Gleason评分通过将前列腺癌组织中最常见的肿瘤形态(主要模式)和第二常见的肿瘤形态(次要模式)分别进行评分,然后相加得出总分。
-
Gleason 6:低度恶性
-
Gleason 7:中度恶性 (3+4或者4+3,前者更危险)
-
Gleason 8-10:高度恶性
-
3. 治疗方式
在治疗前,会对患者进行Risk categories风险评估,选择合适的治疗方式。
- 评估的是"Risk of recurrence",即经过治疗后,癌症又重新复发的可能性
- 基于initial PSA, Cancer stage, PSA density, Gleason scre进行评估
- 主要分为如下类别
- Very Low-risk:T1c,Gleason score<6, PSA < 10等
- Low-risk:T1-T2a, Gleason score≤6,PSA < 10等
- Intermediate risk:T2b-c,Gleason 7,PSA 10-20 ng/mL
- High risk:T3a,Gleason 8-10,PSA>20
- Very High-risk:T3b-T4, Gleason 8-10
下面按局限性与转移性两大类PCa介绍下相应的治疗方式
3.1 局限性PCa
手术或放疗对localized low and intermediate risk PC同样有效;
放疗+激素治疗可用于locally advanced PC
Active surveillance(主动监测)
Chemotherapy (generallly not used in local treatment)
Target therapy (generallly not used in local treatment)
Immunotherapy (generallly not used in local treatment)
手术和放疗是早期前列腺癌(未发生侵袭)的主要手段
(1)Surgery (手术)
- 切除肿瘤在内的整个前列腺组织
- 耻骨后根治性前列腺切除术 (Radical retropubic prostatectomy)
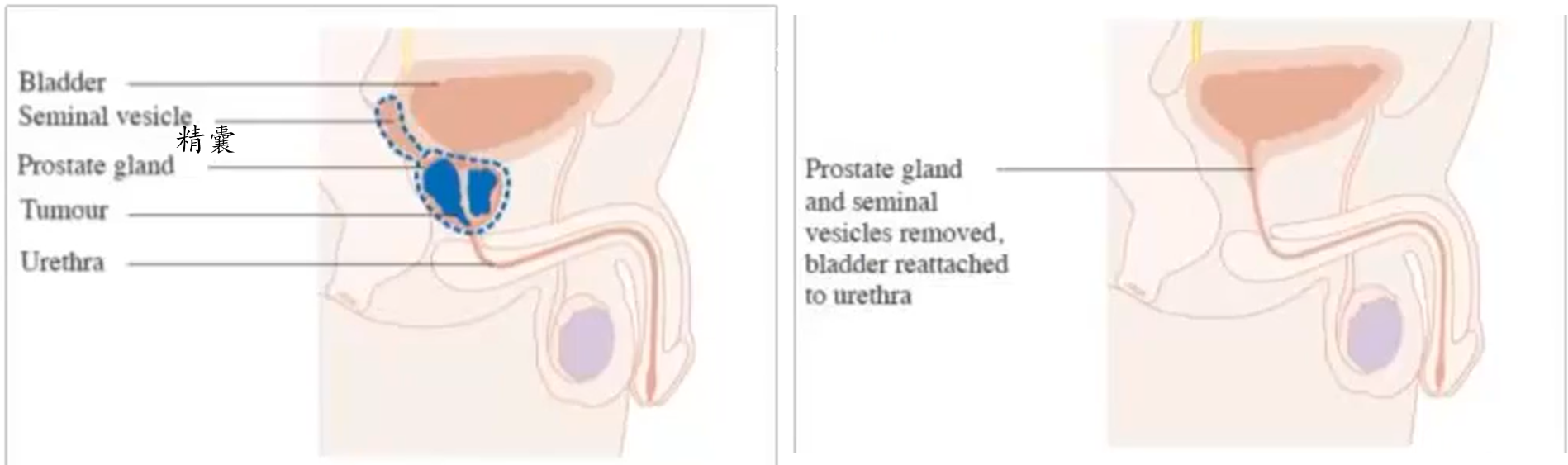
- Neoadjuvant therapy 新辅助治疗(术前)
- 使肿瘤变得更小,更易于手术切除,减少复发的风险,并提高长期生存的可能性。
- Adjuvant therapy 辅助治疗 (术后)
- 消灭任何可能残留的癌细胞,防止癌症复发。
(2)Radiation (放疗)
- 使用X-射线等产生的能量造成DNA损伤,杀伤肿瘤细胞
- 形式上包括外照射放射治疗(External Beam Radiation Therapy, EBRT),近距离放射治疗(Brachytherapy)等
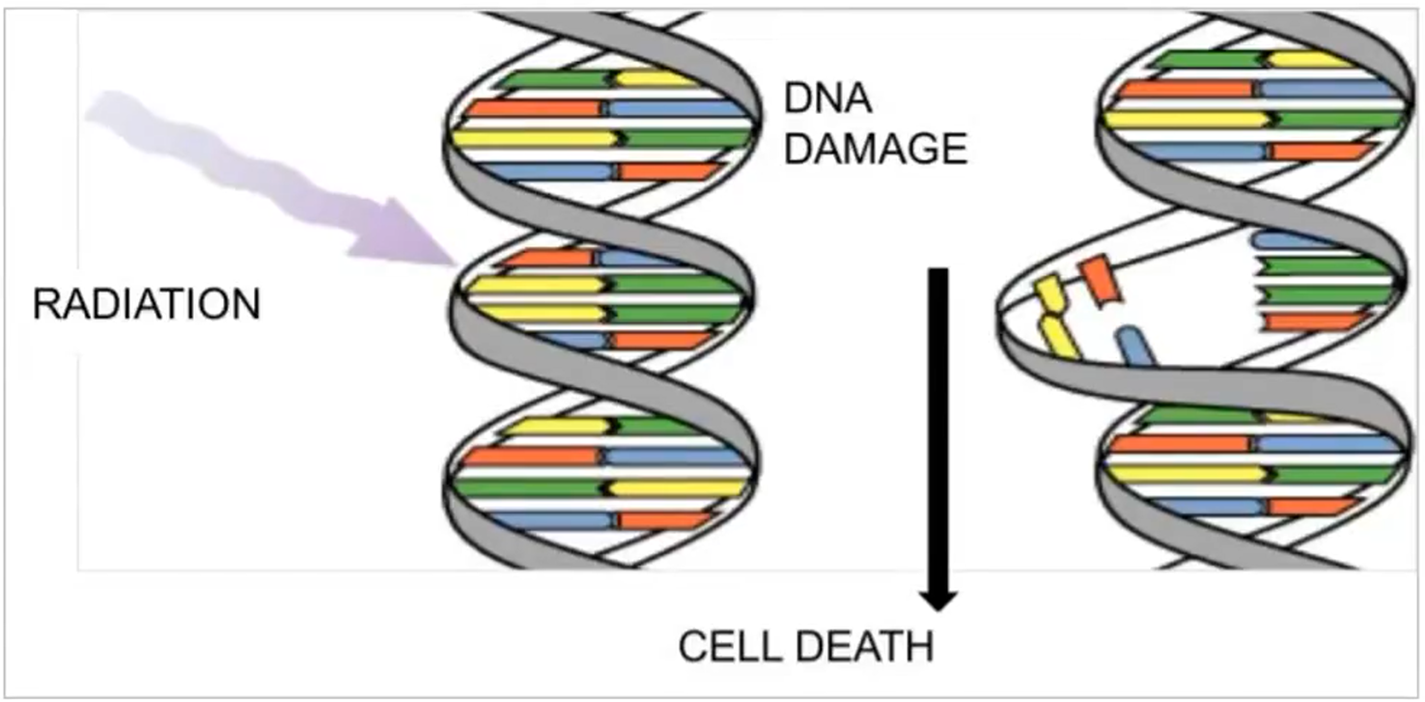
手术或放疗的副作用常包括尿失禁、勃起障碍、消化道相关问题。
(3)Hormone therapy(激素治疗)
-
人体产生的化学物质(激素)告诉每个器官应该做什么,同时也会促进肿瘤生长
-
女性的雌激素(hormone estrogen)控制女性的第二性征发育,包括乳房发育、月经调节等;
- 抗雌激素药物可以用于治疗乳腺癌。
-
男性的睾酮激素(hormone testosterone)负责促进男性生殖器官(如睾丸和前列腺)的发育和生长,还促进肌肉质量增加、骨骼密度增强以及体毛的生长。
- 抗睾酮激素药物可以用于治疗前列腺癌
-
ADT(Androgen Deprivation Therapy)称为雄激素剥夺治疗,通过手术或药物手段来降低雄激素水平或作用。
- 手术层面:主要指手术性阉割(即双侧睾丸切除术);
- 药物层面:如上机制,可以有两种途径:
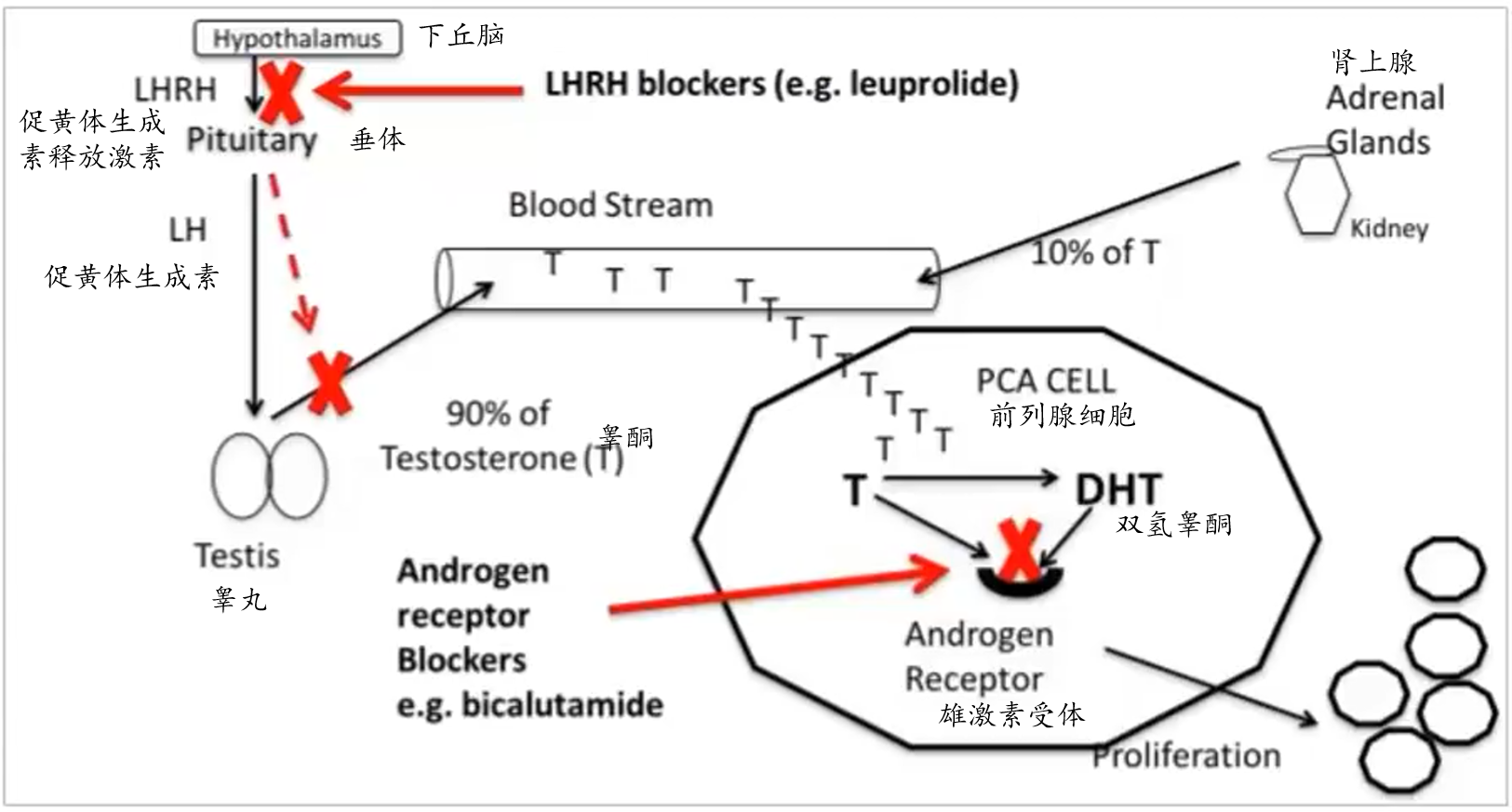
- LHRH阻断剂:抑制垂体前叶分泌LH,从而减少睾丸产生的睾酮量。
- AR阻断剂:占据AR的位置,使真正的雄激素无法与之结合,从而阻止雄激素的信号传导。
睾酮激素调节机制
(1)首先在下丘脑(Hypothalamus),会分泌促黄体生成素释放激素(LHRH,也称为GnRH)。然后这种激素通过垂体门脉系统传递给垂体前叶(Pituitary),刺激垂体前叶产生并释放出促黄体生成素(LH);
(2)血液中的促黄体生成素(LH)到达睾丸(Testis),促进分泌睾酮(T),大约有90%的睾酮与血浆蛋白结合;
(3)当睾酮进入前列腺癌细胞(PCA cell)后,它会被转化为更强效的雄性激素双氢睾酮(DHT)。
(4)睾酮或其衍生物如双氢睾酮(DHT),与靶细胞表面或细胞质内的雄激素受体(AR)结合后,一系列生化反应就会被激活。
- 激素治疗副作用主要由于睾酮激素降低所导致的:
- Hot flash (超热),性欲降低,肌肉减少,骨密度降低,代谢降低(体重增加)等。
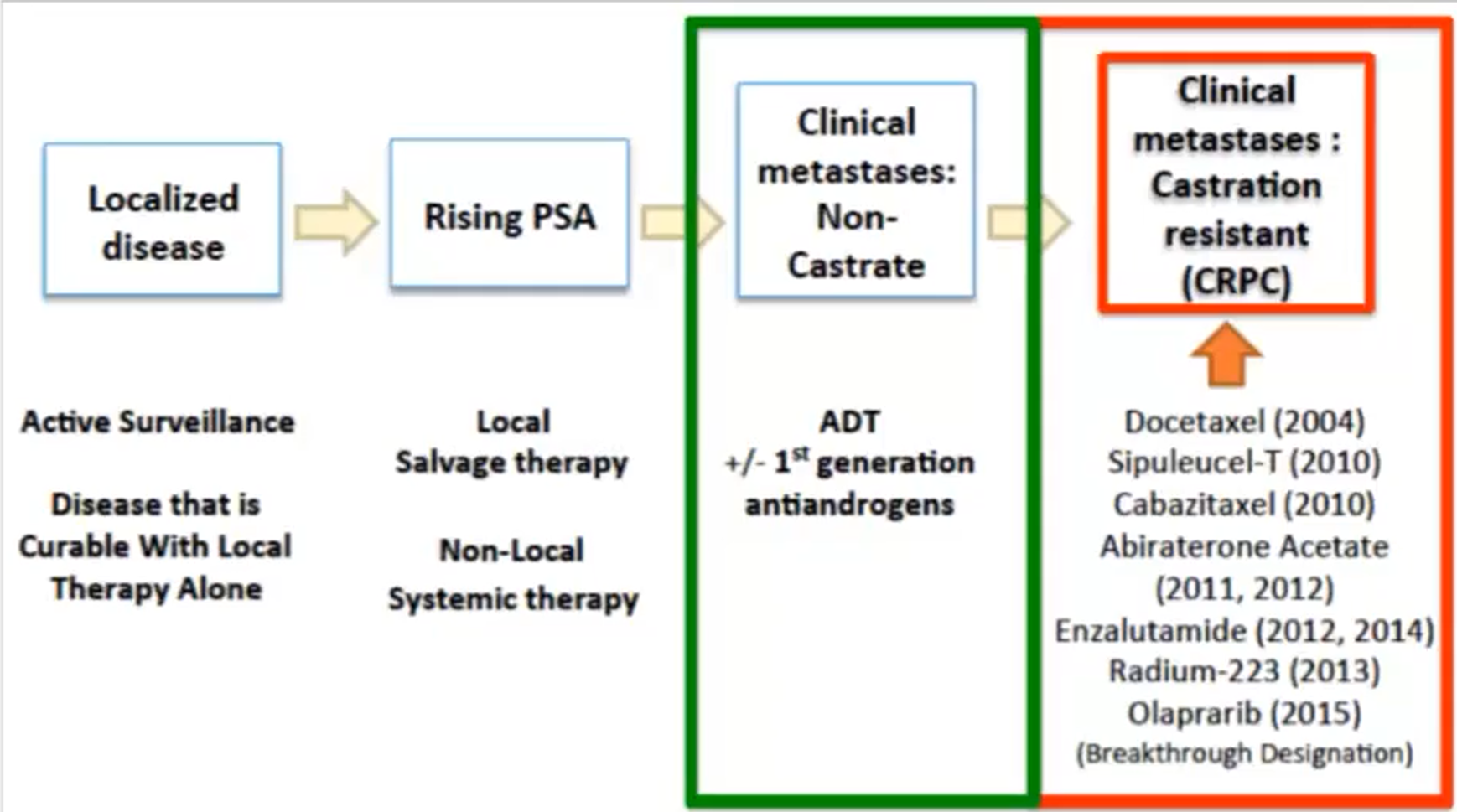
3.2 转移性PC的治疗
PCa最常见的转移形式是骨转移。
(1)激素治疗
-
转移性PCa的一线治疗方案,生存时间5-6年
-
有时联合化疗药物(e.g. Docetaxel多西他赛)取得更佳的效果
-
最终由于耐药性,导致CRPC:Castrate-resistant prostate cancer
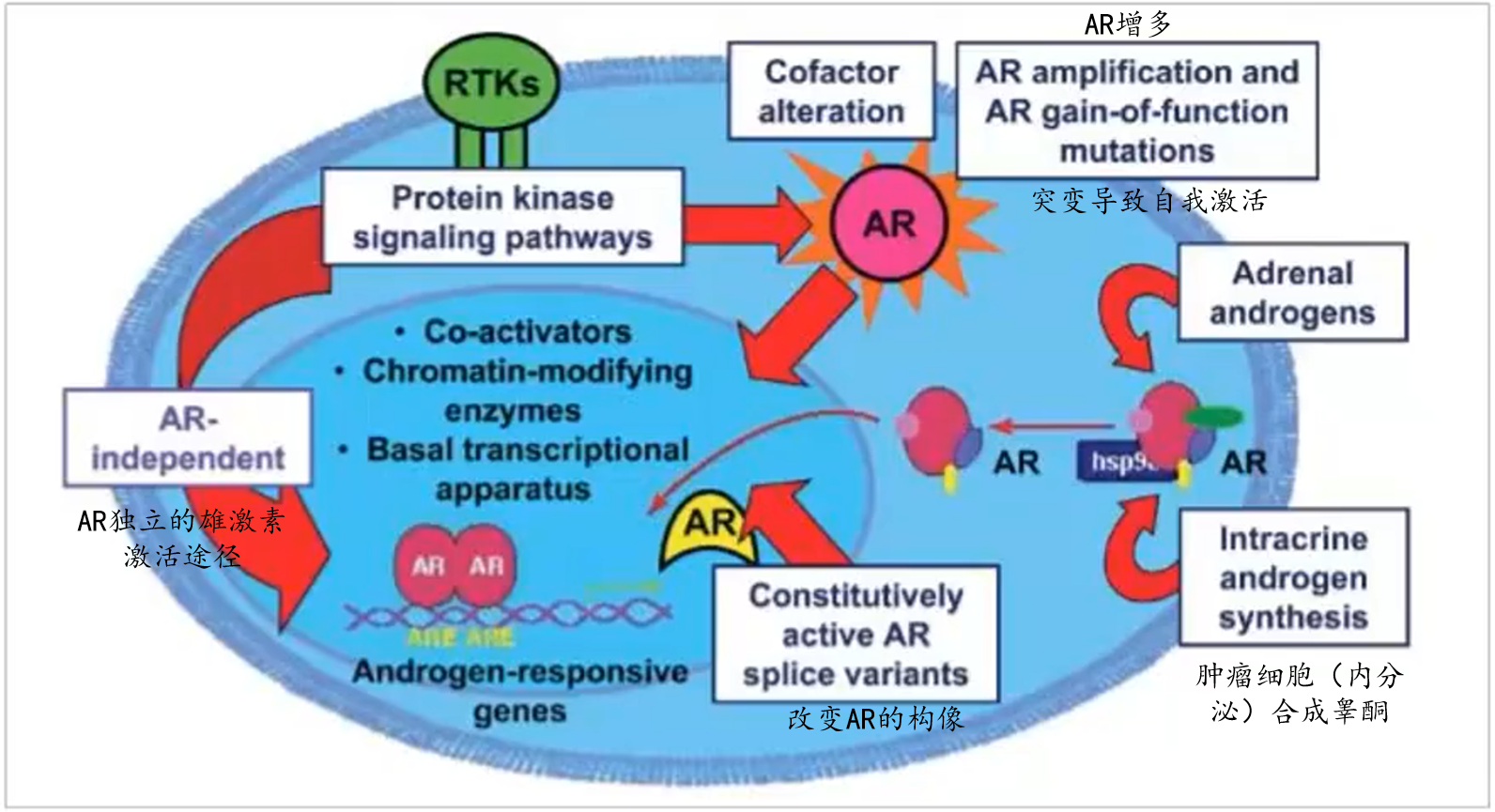
- 目前有多种角度解释,其中最主要的是PCa促进AR(雄激素受体)的增多,使得尽可能利用体内的睾酮激素。
(2)Supra-castration hormonal agents(超去势激素药物)为二线治疗药物
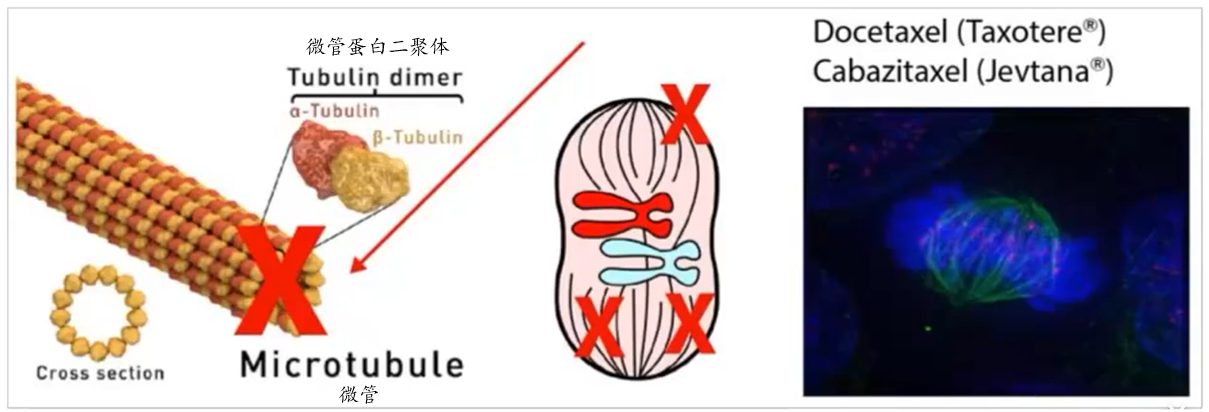
(3)化疗药物,主要有两类
- 干扰有丝分裂 (e.g. 多西他赛,Docetaxel),如下图
- 多西他赛是一线化疗药,用于二线激素治疗失败后
- 副作用主要是损伤正常细胞,例如脱发、食欲不振、恶心等
- 干扰DNA复制 (较少用);
(3)对于骨转移患者的治疗方案最终无效(大部分)时,可以基于driver gene mutation参加临床试验clinical trial (precison medicion)
-
此类研究(targeted gene/pathway以及immune therapy)将在后续阅读文献学习。
-
BRCA2,BRCA2,ATM:19.2%;MLH1,MLH2